Le début du XXe siècle a été une période très propice aux sciences. Outre Ernest Rutherford et Niels Bohr qui ont donné naissance au modèle standard de physique des particules, ce fut également une période de percées dans le domaine de la mécanique quantique. Grâce aux études en cours sur le comportement des électrons, les scientifiques ont commencé à proposer des théories selon lesquelles ces particules élémentaires se comportaient d'une manière qui défie la physique newtonienne classique.
Un tel exemple est le modèle de nuage d'électrons proposé par Erwin Schrodinger. Grâce à ce modèle, les électrons n'étaient plus représentés comme des particules se déplaçant autour d'un noyau central sur une orbite fixe. Au lieu de cela, Schrodinger a proposé un modèle par lequel les scientifiques ne pouvaient que faire des suppositions éclairées quant à la position des électrons. Par conséquent, leur emplacement ne peut être décrit que comme faisant partie d'un «nuage» autour du noyau où les électrons sont susceptibles d'être trouvés.
La physique atomique au XXe siècle:
Les premiers exemples connus de la théorie atomique proviennent de la Grèce antique et de l'Inde, où des philosophes tels que Démocrite ont postulé que toute la matière était composée de minuscules unités indivisibles et indestructibles. Le terme «atome» a été inventé dans la Grèce antique et a donné naissance à l'école de la pensée connue sous le nom d '«atomisme». Cependant, cette théorie était plus un concept philosophique que scientifique.
Ce n'est qu'au 19e siècle que la théorie des atomes s'est articulée comme une question scientifique, avec les premières expériences fondées sur des preuves. Par exemple, au début des années 1800, le scientifique anglais John Dalton a utilisé le concept de l'atome pour expliquer pourquoi les éléments chimiques réagissaient de certaines manières observables et prévisibles. À travers une série d'expériences impliquant des gaz, Dalton a continué à développer ce qu'on appelle la théorie atomique de Dalton.
Cette théorie s'est développée sur les lois de la conversation de masse et de proportions définies et s'est résumée à cinq prémisses: les éléments, dans leur état le plus pur, sont constitués de particules appelées atomes; les atomes d'un élément spécifique sont tous les mêmes jusqu'au dernier atome; les atomes de différents éléments peuvent être différenciés par leur poids atomique; les atomes d'éléments s'unissent pour former des composés chimiques; les atomes ne peuvent être ni créés ni détruits par réaction chimique, seul le groupement change jamais.
Découverte de l'électron:
À la fin du 19e siècle, les scientifiques ont également commencé à théoriser que l'atome était composé de plus d'une unité fondamentale. Cependant, la plupart des scientifiques se sont aventurés sur le fait que cette unité aurait la taille du plus petit atome connu - l'hydrogène. À la fin du 19e siècle, le sien changera radicalement, grâce aux recherches menées par des scientifiques comme Sir Joseph John Thomson.
Grâce à une série d'expériences utilisant des tubes à rayons cathodiques (connus sous le nom de tube de Crookes), Thomson a observé que les rayons cathodiques pouvaient être déviés par des champs électriques et magnétiques. Il a conclu que plutôt que d'être composés de lumière, ils étaient constitués de particules chargées négativement qui étaient 10000 fois plus petites et 1800 fois plus légères que l'hydrogène.

Cela a effectivement réfuté la notion que l'atome d'hydrogène était la plus petite unité de matière, et Thompson est allé plus loin pour suggérer que les atomes étaient divisibles. Pour expliquer la charge globale de l'atome, qui comprenait à la fois des charges positives et négatives, Thompson a proposé un modèle selon lequel les «corpuscules» chargés négativement étaient répartis dans une mer uniforme de charge positive - connue sous le nom de modèle de pudding aux prunes.
Ces corpuscules seront plus tard appelés «électrons», d'après la particule théorique prédite par le physicien anglo-irlandais George Johnstone Stoney en 1874. Et à partir de là, le modèle Plum Pudding est né, ainsi nommé parce qu'il ressemble étroitement au désert anglais qui se compose de gâteau aux prunes et raisins secs. Le concept a été présenté au monde dans l’édition de mars 1904 du Magazine philosophique, à large éloge.
Développement du modèle standard:
Des expériences ultérieures ont révélé un certain nombre de problèmes scientifiques avec le modèle Plum Pudding. Pour commencer, il y avait le problème de démontrer que l'atome possédait une charge de fond positive uniforme, qui est devenue connue sous le nom de «problème Thomson». Cinq ans plus tard, le modèle serait réfuté par Hans Geiger et Ernest Marsden, qui ont mené une série d'expériences utilisant des particules alpha et une feuille d'or - alias. «l'expérience de la feuille d'or».
Dans cette expérience, Geiger et Marsden ont mesuré le modèle de diffusion des particules alpha avec un écran fluorescent. Si le modèle de Thomson était correct, les particules alpha passeraient sans entrave à travers la structure atomique de la feuille. Cependant, ils ont plutôt noté que si la plupart des coups de feu étaient directs, certains d'entre eux étaient dispersés dans différentes directions, certains retournant dans la direction de la source.

Geiger et Marsden ont conclu que les particules avaient rencontré une force électrostatique bien supérieure à celle permise par le modèle de Thomson. Étant donné que les particules alpha ne sont que des noyaux d'hélium (qui sont chargés positivement), cela impliquait que la charge positive dans l'atome n'était pas largement dispersée, mais concentrée dans un volume minuscule. De plus, le fait que les particules qui n'étaient pas déviées passaient sans entrave signifiait que ces espaces positifs étaient séparés par de vastes gouffres d'espace vide.
En 1911, le physicien Ernest Rutherford interprète les expériences de Geiger-Marsden et rejette le modèle de Thomson de l'atome. Au lieu de cela, il a proposé un modèle où l'atome consistait en un espace principalement vide, avec toute sa charge positive concentrée en son centre dans un très petit volume, qui était entouré d'un nuage d'électrons. Ceci est venu pour être connu comme le modèle de Rutherford de l'atome.
Des expériences ultérieures d'Antonius Van den Broek et Niels Bohr ont affiné davantage le modèle. Alors que Van den Broek a suggéré que le numéro atomique d'un élément est très similaire à sa charge nucléaire, ce dernier a proposé un modèle semblable à celui du système solaire de l'atome, où un noyau contient le numéro atomique de charge positive et est entouré d'un égal nombre d'électrons dans les coquilles orbitales (aka. le modèle de Bohr).
Le modèle du nuage d'électrons:
Au cours des années 1920, le physicien autrichien Erwin Schrodinger est devenu fasciné par les théories Max Planck, Albert Einstein, Niels Bohr, Arnold Sommerfeld et d'autres physiciens. Pendant ce temps, il s'investit également dans les domaines de la théorie atomique et des spectres, faisant des recherches à l'Université de Zurich puis à l'Université Friedrich Wilhelm de Berlin (où il succède à Planck en 1927).

En 1926, Schrödinger a abordé la question des fonctions d'onde et des électrons dans une série d'articles. En plus de décrire ce qui allait être connu sous le nom d'équation de Schrodinger - une équation différentielle partielle qui décrit comment l'état quantique d'un système quantique change avec le temps - il a également utilisé des équations mathématiques pour décrire la probabilité de trouver un électron dans une certaine position .
Cela est devenu la base de ce qui allait devenir le modèle du nuage d'électrons (ou mécanique quantique), ainsi que l'équation de Schrodinger. Basé sur la théorie quantique, qui affirme que toute la matière a des propriétés associées à une fonction d'onde, le modèle de nuage d'électrons diffère du modèle de Bohr en ce qu'il ne définit pas le chemin exact d'un électron.
Au lieu de cela, il prédit la position probable de l'emplacement de l'électron en fonction d'une fonction de probabilités. La fonction de probabilité décrit essentiellement une région semblable à un nuage où l'électron est susceptible d'être trouvé, d'où le nom. Là où le nuage est le plus dense, la probabilité de trouver l'électron est la plus élevée; et là où l'électron est moins susceptible d'être, le nuage est moins dense.
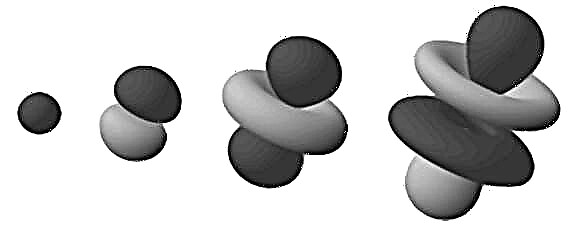
Ces régions denses sont appelées «orbitales électroniques», car elles sont l'endroit le plus probable où un électron en orbite sera trouvé. En étendant ce modèle de «nuage» à un espace tridimensionnel, nous voyons un haltère ou un atome en forme de fleur (comme dans l'image en haut). Ici, les régions de ramification sont celles où nous sommes le plus susceptibles de trouver les électrons.
Grâce aux travaux de Schrodinger, les scientifiques ont commencé à comprendre que dans le domaine de la mécanique quantique, il était impossible de connaître la position exacte et la quantité de mouvement d'un électron en même temps. Indépendamment de ce que l'observateur sait initialement d'une particule, il ne peut prédire sa localisation ou son élan en termes de probabilités.
À aucun moment, ils ne pourront vérifier ni l'un ni l'autre. En fait, plus ils en sauront sur la quantité de mouvement d'une particule, moins ils en sauront sur son emplacement, et vice versa. C'est ce que l'on appelle aujourd'hui le «principe d'incertitude».
Notez que les orbitales mentionnées dans le paragraphe précédent sont formées par un atome d'hydrogène (c'est-à-dire avec un seul électron). Lorsqu'il s'agit d'atomes qui ont plus d'électrons, les régions orbitales des électrons se répartissent uniformément en une boule floue sphérique. C’est là que le terme «nuage d’électrons» est le plus approprié.
Cette contribution a été universellement reconnue comme étant l'une des contributions les plus importantes en termes de coûts du 20e siècle, et qui a déclenché une révolution dans les domaines de la physique, de la mécanique quantique et, en fait, de toutes les sciences. Désormais, les scientifiques ne travaillent plus dans un univers caractérisé par des absolus de temps et d'espace, mais par des incertitudes quantiques et une relativité spatio-temporelle!
Nous avons écrit de nombreux articles intéressants sur les atomes et les modèles atomiques ici à Space Magazine. Voici quel est le modèle atomique de John Dalton?, Quel est le modèle du pudding aux prunes?, Quel est le modèle atomique de Bohr?, Qui était Démocrite?, Et quelles sont les parties d'un atome?
Pour plus d'informations, assurez-vous de vérifier Qu'est-ce que la mécanique quantique? de Live Science.
Astronomy Cast a également un épisode sur le sujet, comme l'épisode 130: Radio Astronomy, l'épisode 138: Quantum Mechanics et l'épisode 252: Heisenberg Uncertainty Principle